致力于为患者开发新药的生物制药公司 Verastem Oncology 今天宣布,美国食品和药物管理局 (FDA) 已授予 RAF/MEK 抑制剂 avutometinib 与选择性 FAK 抑制剂 defactinib 联用治疗胰腺癌的孤儿药认定 (ODD)。

Verastem Oncology 总裁兼首席执行官 Dan Paterson 表示:“在 ASCO 2024 年度会议上,我们报告了正在进行的 RAMP 205 试验的积极初步中期结果,该试验评估了 avutometinib 和 defactinib 与标准护理化疗联合治疗一线转移性胰腺癌的效果。”FDA 将avutometinib 和 defactinib联合用于治疗胰腺癌的孤儿药指定为认识到胰腺癌患者的大量未满足的治疗需求。我们相信,avutometinib 和 defactinib与标准治疗相结合,有机会为治疗这种具有挑战性的癌症提供一种不同的方法。我们期待着在 2025 年第一季度正在进行的 RAMP 205 试验中报告跨剂量队列的最新数据。”
在 2024 年 6 月举行的美国临床肿瘤学会 (ASCO) 年会上,Verastem 展示了正在进行的 RAMP 205 试验的初步中期安全性和有效性结果,该试验将 avutometinib 和 defactinib 与当前治疗标准吉西他滨和白蛋白结合型紫杉醇联合用于一线治疗转移性胰腺癌。截至 2024 年 5 月 14 日数据截止,已有 41 名患者接受了四个剂量队列方案之一的治疗,只有剂量队列 1 中的患者至少接受了六个月的随访。在剂量水平 1 队列中,83% (5/6) 的患者在数据截止时经过六个月以上的随访获得了确认的部分缓解。在剂量水平 1 队列中观察到一种剂量限制性毒性 (DLT),随后在招募更多患者后清除了剂量水平。在所有队列中的 26 名患者中,有机会在治疗期间进行第一次扫描,其中 21 名患者的目标病灶直径总和的变化有所减少。
关于Avutometinib和Defactinib的联用
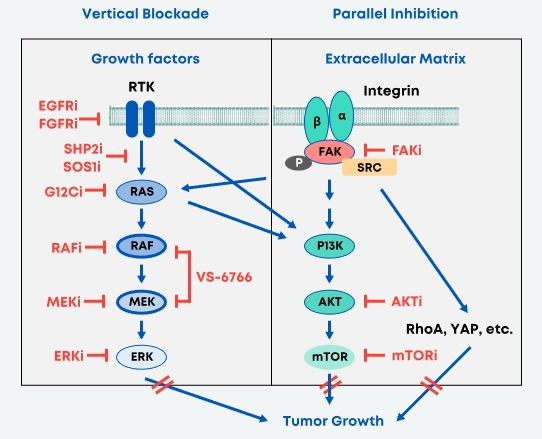
Avutometinib 是一种 RAF/MEK 钳夹,可诱导 MEK 与 ARAF、BRAF 和 CRAF 的无活性复合物,通过最大限度地抑制 RAS/MAPK 通路,可能产生更完整和持久的抗肿瘤反应。与目前可用的仅含 MEK 的抑制剂相比,Avutometinib 可阻断 MEK 激酶活性和 RAF 磷酸化 MEK 的能力。这种独特的机制允许阿武替尼阻断 MEK 信号传导,而无需补偿激活 MEK,这似乎限制了其他仅使用 MEK 的抑制剂的疗效。美国食品和药物管理局(FDA)批准了突破性治疗指定,将Avutometinib 和Defactinib(一种选择性 FAK 抑制剂)的研究组合用于治疗所有复发性低级别浆液性癌症(LGSOC)患者,无论其在一种或多种先前的治疗方案(包括基于铂的化疗)后的 KRAS 状态如何。Avutometinib 单独或与 defactinib 联合使用也被美国食品药品监督管理局授予孤儿药指定,用于治疗 LGSOC。
Verastem Oncology 公司目前正在进行 avutometinib 在 RAS/MAPK 驱动的肿瘤中的临床试验,作为其 RAF 和 MEK 计划或 RAMP 的一部分。RAMP 301(NCT06072781)是一项国际 3 期验证性试验,旨在评估阿武美替尼和 defactinib 联合治疗与标准化疗或激素治疗治疗复发性 LGSOC 的比较。RAMP 201(NCT04625270)是一项在复发性 LGSOC 患者中进行的 avutometinib 联合 defactinib 的 2 期注册指导试验,在剂量优化和扩展阶段以及低剂量评估中均已完成招募。Verastem 已开始为患有复发性 LGSOC 的成人患者提交 avutometinib 和 defactinib 组合的滚动新药申请,预计将于 2024 年下半年完成新药申请,FDA 可能于 2025 年上半年做出决定。
Verastem Oncology 已与 Amgen 和 Mirati 建立临床合作,作为 RAMP 203 (NCT05074810) 和 RAMP 204 的一部分,评估 LUMAKRAS ™ (sotorasib) 联合 avutometinib 和 defactinib 以及 KRAZATI ™ (adagrasib) 联合 avutometinib 治疗 KRAS G12C 突变 NSCLC (NCT05375994) 试验分别。RAMP 205 (NCT05669482) 是一项 1b/2 期临床试验,评估 avutometinib 和 defactinib 联合吉西他滨/白蛋白结合型紫杉醇治疗一线转移性胰腺癌患者,该试验得到了 PanCAN 治疗加速器奖的支持。
前瞻性陈述
本文包含前瞻性陈述。前瞻性陈述的标志性词语包括"预期"、"应"、“估计”、"可能"、"会"、“将”、“相信”、“将来”、“计划”以及类似表达。前瞻性陈述通常涉及不受本公司控制的风险及不确定性因素,可能导致实际结果与前瞻性陈述的预期结果完全不符。任何人需审慎考虑风险及不确定性因素,不可完全依赖本文的“前瞻性陈述”。本公司声明,无论是否出现最新信息、未来事件或其它情况,本公司均无义务对任何前瞻性陈述进行更新或修改。
内容来自中国SFDA,美国FDA,药品审评中心、国家基本医保目录等权威部门,部分内容来自互联网,如涉及医学知识、观点、建议都不应被视为医生建议或处方诊断,所有信息仅供参考,康和医药不对其承担任何责任,如有错误,版权问题请来电来函告知。